Procedimiento numérico
Gas ideal bidimensional
En esta página, se comentan los pasos esenciales para crear la simulación del experimento que nos permite comprobar la fórmula de la distribución de las velocidades moleculares. Se emplea un modelo de gas bidimensional
Volvemos sobre la distribución de las velocidades moleculares. El número de moléculas cuya velocidad está comprendida entre v y v+dv, o bien entre vx y vx+dvx, vy y vy+dvy de acuerdo a la ley de Boltzmann es
donde c es una constante a determinar sabiendo que el número total de moléculas es N.
Se efectúa una integral doble entre los límites -∞ y +∞ , teniendo en cuenta el resultado de la integral
El resultado es
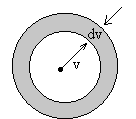 En el espacio de velocidades del gas bidimensional,
el elemento de área, es el área del anillo comprendido entre las
circunferencias de radio v y v+dv. dv=2π vdv, tal como se ve en la figura
En el espacio de velocidades del gas bidimensional,
el elemento de área, es el área del anillo comprendido entre las
circunferencias de radio v y v+dv. dv=2π vdv, tal como se ve en la figura
El número de partículas cuyo módulo de la velocidad está comprendida entre v y v+dv es
donde T es la temperatura relacionada con la velocidad media <v> de las N moléculas del gas ideal bidimensional.
La velocidad media <v> de las moléculas del gas bidimensional está relacionada con su temperatura T.
Para deducir estas expresiones, se han empleado el resultado de las integrales
Para generar la distribución de las velocidades de las moléculas de un gas ideal bidimensional, se emplean los métodos de Montecarlo.
Se genera números aleatorios γ, uniformemente distribuidos en el intervalo [0, 1), para cada número γ se obtiene la velocidad de una molécula de acuerdo con la siguiente fórmula
La ventaja de utilizar este modelo, es que la integral es inmediata y se despeja fácilmente v.
Finalmente, se sitúa cada molécula en el tambor, en la posición dada por la relación de transformación
