Medida del coeficiente de difusión

Se dispone de un tubo delgado de algunos centímetros de largo y de uno o dos milímetros de diámetro. Se llena con un líquido volátil tal como éter, acetona o tetracloruro de carbono. A medida que el líquido se evapora, desciende el nivel de la columna de líquido. El experimento consiste en medir la distancia h entre el extremo superior del tubo y la parte inferior del menisco en función del tiempo t.
Una gráfica de h en función de la raíz cuadrada del tiempo t da una línea recta. A partir de la pendiente de la recta, se obtiene el coeficiente de difusión D.
Existe un proceso de difusión siempre que se establezca un gradiente de concentración.
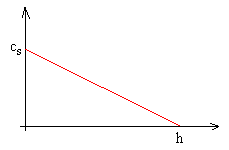
La concentración de vapor decrece desde su valor cs en la superficie del líquido a cero en el extremo abierto del tubo, donde el vapor es arrastrado por las corrientes imperceptibles de aire que siempre están presentes. El gradiente de concentración es por tanto, cs/h, siendo cs la concentración de vapor saturado.
El descenso del nivel del líquido es suficientemente lento, para considerar el proceso de difusión como cuasi-estacionario. La situación análoga la hemos estudiado en el fenómeno de la conducción del calor por una barra metálica. Cuando se alcanza el estado estacionario, la distribución de temperaturas a lo largo de la barra no cambia con el tiempo sin embargo, hay un flujo constante de calor desde el extremo caliente al frío que es proporcional al gradiente de temperatura.
De acuerdo con la ley de Fick, el flujo JA (masa de vapor que atraviesa la sección A del tubo en la unidad de tiempo) es proporcional al gradiente de concentración. La constante de proporcionalidad se denomina coeficiente de difusión D.
La masa de vapor que atraviesa la sección A del tubo en la unidad de tiempo JA, será igual a la masa de líquido evaporado en la unidad de tiempo. Si A·dh es el volumen evaporado en el tiempo dt y ρ es la densidad del líquido
Llegamos a la ecuación
Integramos con las condición inicial siguiente: en el instante t=0, h=0, que da
La concentración de vapor saturado cs se puede determinar a partir de los datos de la presión de vapor saturado ps que suministran las tablas. Suponiendo que el vapor saturado se comporta como un gas ideal
Siendo m la masa (en gramos) del gas y V su volumen (en litros), la concentración cs=m/V en (g/cm3). La presión de vapor ps se suele dar en mm de mercurio (torr), 1/760 de una atmósfera y la temperatura en kelvin, de modo que la concentración de vapor cs se calcula mediante la siguiente fórmula
Datos de los líquidos
| Líquido | Peso molecular (g) | Densidad (g/cm3) | Coef. difusión cm2/s |
|---|---|---|---|
| Acetona | 58.1 | 0.792 | 0.101 |
| Éter | 74.12 | 0.7135 | 0.091 |
| Tetracloruro de carbono | 153.8 | 1.595 | 0.079 |
Datos de la presión de vapor saturado ps (torr) para varias temperaturas
| Líquido | 10ºC | 15ºC | 20ºC | 25ºC | 30ºC |
|---|---|---|---|---|---|
| Acetona | 115.6 | 147.1 | 184.8 | 229.2 | 282.7 |
| Eter | 291.7 | 360.7 | 442.2 | 537.0 | 647.3 |
| Tetracloruro de carbono | 53.1 | 68.7 | 86.5 | 109 | 137 |
En general, el coeficiente de difusión D cambia con la temperatura, pero por razón de simplicidad supondremos que se mantiene constante en el intervalo de temperaturas estudiado.
Actividades
Se elige
- El líquido (acetona, éter o tetracloruro de carbono) en el control titulado Líquido
- La temperatura (10, 15, 20, 25 ó 30ºC) del líquido en el control titulado Temperatura
Se pulsa el botón titulado Nuevo
Se observa como el líquido volátil elegido se va evaporando a la vez que va descendiendo la columna de fluido. Las moléculas de vapor se difunden desde la superficie del líquido por el aire a lo largo de la columna hasta su extremo superior. La concentración de vapor es máxima cs en la superficie de líquido y es nula en el extremo abierto del tubo.
Una gráfica situada al lado del tubo vertical, representa en el eje vertical la altura h (cm), o distancia entre el extremo del tubo abierto y el menisco de fluido, en el eje horizontal la raíz cuadrada del tiempo expresado en minutos.
Para que los puntos en la gráfica estén igualmente espaciados a lo largo del eje horizontal se toman los datos de la altura h en los instantes t=1, 4, 9, 16, 25… minutos.
El programa interactivo nos suministra el valor de la pendiente de la recta que pasa por los puntos “experimentales” a partir de la cual, calculamos el coeficiente de difusión D.
Ejemplo:
Se llena el tubo de acetona y se mantiene a la temperatura constante de 10ºC=283 K.
Cuando se completa la “experiencia” tomamos el dato de la pendiente de la recta y nos da
A partir de los datos de las tablas, obtenemos la concentración cs de vapor saturado a dicha temperatura
Conocida la pendiente a de la recta, se despeja el coeficiente de difusión D
D=0.101 cm2/s=1.01·10-5 m2/s
Referencias
Pryde J. A., Pryde E. A. A simple quantitative diffusion experiment. Physics Education, Vol 2 (1967) pp. 311-314

