Enfriamiento de un gas
Imaginemos un gas compuesto por N0 moléculas que ocupan un recipiente a la temperatura T0. La distribución de equilibrio es
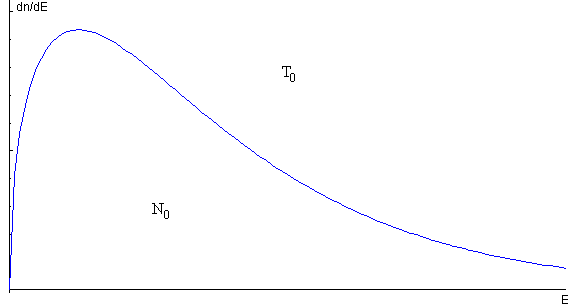
Por algún procedimiento (véase el artículo citado en las referencias) se eliminan del recipiente todas las moléculas que se muevan con una velocidad superior a vc o tengan una energía superior a Ec (en color azul en la figura) quedando N1 moléculas en el recipiente.
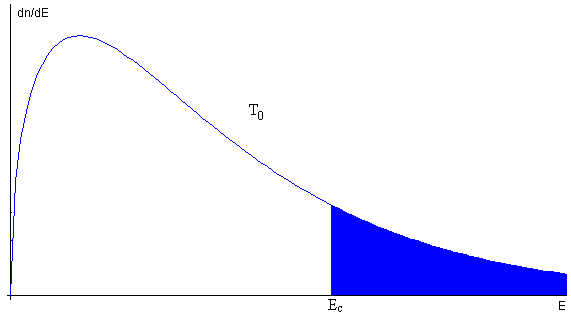
Las N1 moléculas que permanecen en el recipiente están inicialmente en una situación de no equilibrio tal como se muestra en la figura, más abajo
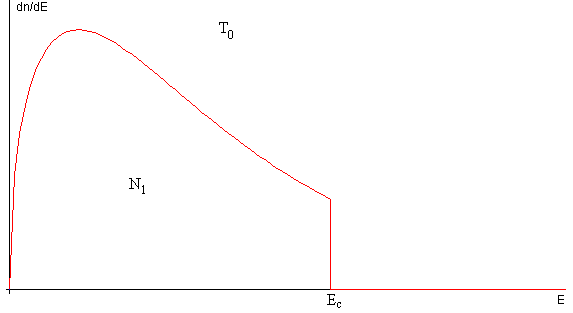
Las N1 moléculas que permanecen en el recipiente chocan entre sí y vuelven a adoptar la distribución de equilibrio a una temperatura inferior T1
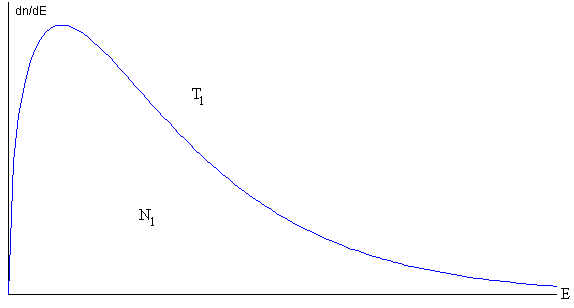
La energía antes y después alcanzar la distribución de equilibrio no cambia, de modo que
Dada la energía Ec podemos calcular la temperatura T1 de las N1 moléculas del gas que permenecen en el recipiente.
La integral de la derecha, la hemos resuelto en la página anterior, al calcular la energía interna U de N moléculas de un gas a la temperatura T
Sustituimos N1 y despejamos T1
Hacemos el cambio de variable x=E/kT
El número de partículas que permanece en el recipiente es
La temperatura T1 del gas compuesto por N1 moléculas es
Resolvemos la integral del denominador
Se hace el cambio de variable y2=x
Se integra por partes
Resolvemos la integral del numerador
La temperatura T1 es
El número de moléculas
Actividades
Se introduce
- La temperatura inicial del gas T0 en el control de edición titulado Temperatura (K)
Se pulsa el botón titulado Nuevo
Se representa la función de distribución de las moléculas dn/dE con la energía E expresada en electrón-voltios eV
- La energía Ec de corte o mínima de las moléculas que se van a eliminar del recipiente, en el control de edición titulado Energía
Se pulsa el botón Eliminar
La proporción de moléculas que van a ser eliminadas, es el cociente entre el área bajo la curva de la distribución señalada en color azul y el área total bajo la curva.
Se proporciona el dato de la proporción de moléculas eliminadas en la parte superior derecha del applet.
Se pulsa el botón titulado Equilibrio
La distribución inicial de no equilibrio, se convierte en una distribución de equilibrio a una temperatura inferior, debido a los choques entre las molécula del gas contenido en el recipiente.
Se proporciona el dato de la nueva temperatura T1 y de la proporción de moléculas que permanecen en el recipiente, N1.
Se compara la distribución de equilibrio a la temperatura T0 (en color gris) con la distribución actual a la temperatura T1 (en color azul).
El estado final es el estado inicial para una nueva iteracción. Se introduce una nueva energía de corte Ec (o se mantiene el mismo valor), se pulsa el botón Eliminar y a continuación, el botón titulado Equilibrio. De este modo, vamos enfriando el gas a la vez que van eliminando las moléculas más energéticas del mismo.
Los pares de datos, (T1, N1) se guardan el en área de texto situado a la izquierda del applet hasta un máximo de 15. Cuando se completa la experiencia se pulsa el botón Gráfica. Se representa los "datos experimentales", temperatura en el eje horizontal, proporción de átomos que permenecen en el recipiente en el eje vertical.
Referencias
Henn E. A., Seman J. A., Ramos E. R. F., Iavaronni A. H., Amthor T., Bagnato V. S., Evaporation in atomic traps: A simple approach. Am. J. Phys. 75 (10) October 2007, pp. 907-910
